もうひとつのパンデミックー鳥インフルエンザ
コロナウィルスで大騒ぎしているが、新型コロナ以前からずっと続いているパンデミックがある。鳥の世界のパンデミック「鳥インフルエンザ」だ。
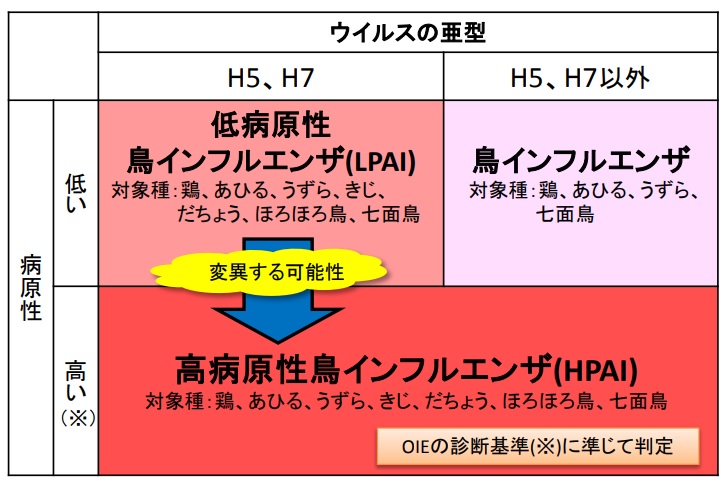
鳥インフルエンザは1950年代にA型インフルエンザとして分類されて以降、世界中で様々な型がひろがっている。鳥のA型インフルエンザはH5,H7型(低病原性トリインフルエンザと、それが変異した高病原性鳥インフルエンザとがある)と、それ以外の鳥インフルエンザに分けられる。
1950年以降の、世界のH5,H7型高病原性鳥インフルエンザの発生状況をみると、当初は数年おきだったものが2000年以降は毎年各地で発生が報告されており、いまだに終息の気配はない。
低病原性だったH5,H7型が変異して高病原性になれば、ほぼ100%の鳥は死ぬ。
H5,H7型以外は家禽にとって重要な病原体とは見なされおらず、OIEもこれ以外は各国に報告することを求めていない。しかし近年、H5、H7以外の、H3N1ウイルスが、重大な問題をひきこ起こす可能性が明らかになっている。繁殖用鶏では死亡率60%、採卵鶏では40%まで死亡率が上昇し、回復後も、産卵能力が完全には回復しなかったという JULY 29, 2020 Avian flu: ever-changing threat to poultry health )
2013年から2017年の間だけでも、高病原性鳥インフルエンザで死亡あるいは殺処分された家禽(家畜化された鳥)は117,789,579羽*、2005年から2021年までの間の死亡、殺処分を合計すると263,012,167羽**だ(2021年5月時点なので、2021年のデータはすべて集計されていない)**。
*OIE Situation Report for Avian Influenza Latest update: 25/01/2018
**OIE WAHISから算出
コロナよりも深刻な状況だが、鳥の世界の問題だと他人事のようには言っていられない。専門家たちはずいぶん前から鳥の間のH5,H7型がヒト-ヒト間で感染することができる「新型」へ変異する可能性を危惧しているからだ。これまで起きた新型インフルエンザのパンデミックはおよそ10-40年おきに発生してるので、次のパンデミックに備えなければならない時期はすでに来ている。
これまでの新型インフルエンザ
1918年 スペインインフルエンザ
1957-58年 アジアインフルエンザ
1968-69年 ホンコンインフルエンザ
2009-2010年 インフルエンザ2009(いわゆる豚インフルエンザ)
*いずれもA型インフルエンザ。A型はヒトと動物に感染する、B型はヒトのみ。C型はブタとヒトに感染するが軽微だと言われている。またA型インフルエンザはH5N8などのように表されるが、Hには「H1~H16」の16種類の形、Nには「N1~N9」の9種類の形が知られている。
厚生労働省はこれら過去のデータをもとに、次に起こる新型インフルエンザのパンデミックを想定している。それによると日本人口の最大25%(約3,200万人)がり患し、約17万人-64万人が死亡する*。ただ厚生労働省が参考にした過去の新型インフルエンザはいずれもH5,H7以外の弱毒性の鳥インフルエンザだ。家禽の間で現在パンデミックを起こしているH5,H7型の高病原性鳥インフルエンザがヒト間で感染可能な新型に変異した場合、この想定された数字は大きく上昇するのではないだろうか。
*新型インフルエンザにおける被害想定について 厚生労働省健康局結核感染症課 新型インフルエンザ対策推進室
なぜウィルスが強毒性になるのか
H5,H7型を含めたA型インフルエンザの元をたどれば水鳥にいきつく。自然宿主である水鳥はA型インフルエンザウィルスと共存しており病気にならない、あるいはなったとしても軽症だ。家禽(家畜化された鳥)にH5、H7型がうつった時も初めは毒性が低い(低病原性)。それがなぜ100%の致死率で何億もの家禽を死に至らしめるほどの強毒性を持つ高病原性に変異するのだろうか。
1959年-2015年の間にH5,H7型が低病原性から高病原性へ転換した39の事例を調査したレポート(2018年*)によると、転換したH5,H7型のうち2つが昔ながらの裏庭養鶏(裏庭で放し飼いする昔ながらの小規模な養鶏)で発生したもので、残りの37は工場型の飼育密度の高い家禽農場で起こったものであることがわかった。
このことは、これまで1950年代以降の高病原性鳥インフルエンザがどういった国を中心に発生してきたのかということとも合致する。高病原性鳥インフルエンザの発生は畜産動物を工場型に多頭飼育する先進国に多いのだ。
飼育密度が高いと副腎肥大が生じることがわかっており、高い飼育密度で飼育される鶏は免疫不全の可能性があることが示唆されている。低めの飼育密度(10または14羽の鳥/m²)で飼育された鳥は、18羽/m²で飼育された鳥よりもニューカッスル病に対する抗体反応が大きいことも分かっている*。しかし現代の畜産では、家禽は高密度で飼育されることが一般的だ。
*Dec 9, 2020 Effects of stocking density on broiler production parameters
次々と感染伝播し、感染した動物の中で増殖と変異を繰り返すうちにウィルスは強い伝染性と強毒性を持つようになる。畜舎にはストレスで免疫力が落ち、溜まった糞尿から出るアンモニアで呼吸器を患う動物が数万単位で過密飼育されている。しかも家畜は徹底した育種で遺伝的に同一で多様性はない。感染を遅らせるための免疫防壁は取り除かれている状態だ。増殖の過程で変異を起こすウィルスにとって、進化するのにこれほど適した繁殖場はないといえるだろう。
家禽農場から他の種への伝染
家禽農場で強毒性を持ったH5,H7型で、他の種への感染が確認されているものがいくつかある。いずれの型もヒトへ感染し強毒性を示しており、その中でもH5N1型ではネコ,ネズミ,イヌ,ウサギ,ブタへ感染して示し死に至らしめている。
持続的なヒト-ヒト間の感染はまだ確認されていないがウィルスは刻々と変異しており予断は許されない。たとえばH7N9型は、はじめは低病原性だったものが2016年後半に変異し高病原性となり、さらにヒト型のレセプターに結合できるよう変異している。現に2020年に発生した北アイルランドの低病原性鳥インフルエンザでは甚大な被害が出ている。 Sep 24, 2021 Disease control challenges of non-notifiable LPAI
*以下は、鳥インフルエンザが家禽から人に感染したすべての事例ではない。
H7N9型
感染が確定した者:1,568名、死亡者:616名*
*H7N9 situation update 04 December 2019, 17:00 hours; Rome
H5N1型
感染が確定した者:861名、死亡者:455名。
862 例。これらの症例は 17 か国からのもので、約 76% がエジプトとインドネシア*。
*Cumulative number of confirmed human cases for avian influenza A(H5N1) reported to WHO, 2003-2020
H5N8型
2021年2月21日、ロシアで初めて高病原性鳥インフルエンザウイルス(H5N8亜型)のヒトへの感染が確認された。これは日本で2020-2021年に猛威を振るった鳥インフルエンザと同じ型でもある。
ロシア、鳥インフルH5N8亜型のヒト感染を確認 世界初 2021年2月21日
他にも、中国で散発的に発生しており、公衆衛生上も大きな問題となっている、H5N6型も、患者が発病前に家きんに曝露したり、生きている家きんの市場を訪れたりしている。
豚を介してパンデミックになる可能性
鳥のウィルスが種の壁を超えて直接ヒトーヒト間のパンデミックにつながることはおそらくない。
これまでの新型インフルエンザのパンデミックには中間宿主が存在した。それは豚だと考えられている。豚は鳥と人の中間の体温を持ち、鳥と人両方のウィルスにかかりやすく、両方の遺伝子の交雑が容易におこるからだ。ある調査では豚の体からみつかった400のウィルスの8割近くが、人や鳥のインフルエンザウィルスの遺伝子が混ざっていたという。
これまで人に感染して死にいたらしめた鳥インフルエンザH5N1型とN7N9型は、直接鳥から人へと伝播したとされている。だがそこからさらにヒト-ヒト間で持続的な感染ができるようになるためにはもう一つ壁を乗り越えなければならない。その壁を突破するために豚が介在する可能性はあるだろう。
豚もまた七面鳥や鶏たち家禽類と同じく、多頭飼育の過密な工場畜産で飼育されている。1998年に豚に感染する豚のインフルエンザウィルスと鳥のインフルエンザウィルス、人のインフルエンザウィルスの混ざった三種混雑ウィルスが発見された時、研究者らは「工場型畜産施設を温床に病原体が生じ、職員や獣医からやがて一般人にまで広がって世界流行を引き起こすおそれがある」と警告したが、有効な手は打たれなかった。そのウィルスがその後さらに別のウィルスは遺伝子交雑して2009-2010年のインフルエンザ2009(いわゆる豚インフルエンザ)パンデミックにつながった*。
アイオワ大学公衆衛生学院の新興感染症センター所長を務めるグレゴリー・グレイは、インフルエンザなどの呼吸器系ウィルスについて次のように言う。
呼吸器系ウィルスがこうした監禁施設に入ると遺伝子の複製・変異・再集合、組み換えを続けて新型になる機会を得られる。人間集団の中で最適な繁殖源はどこかといえば、監獄・軍事基地・船・学校などがあげられよう。但し、これらの人間集団内では呼吸器系ウィルスは即座に広まってまた収まるのに対し、CAFO(工場型畜産施設)では動物が繰り返し外から持ち込まれることが珍しくないので、ウィルスが拡散して流行病になる可能性ははるかに高い。
新型インフルエンザのパンデミックを防ぐには
畜産に関わる産業界は工場型の畜産方式がウィルス増殖の温床になっていることを知っているはずだ。それが新型に変異してヒト間に感染してパンデミックを起こす可能性についても気付いている人はいるだろう。
だが何ら手を打たず今の業態を継続している。それは社会の混乱よりも自分たちの利益を優先しているからにほかならない。産業界だけではない。工場型畜産から生産された肉や卵を食べる人々も責任を逃れることはできない。
次の新型インフルエンザでパンデミックが起こった時にどうするのかという議論は行われていても、インフルエンザが新型に変異しやすい環境とは何か?その環境をつくらないためにどうすればいいのかという議論はみかけない。このままではおそらくコロナに続き新型インフルエンザのパンデミックは起こる。そしてそれが家禽農場で強毒性を持ったH5,H7型に由来するものであれば現在のコロナどころではない混乱となるだろう。
人々がはじめてウィルスの温床となっている工場型畜産に目を向けるのは、パンデミックがおこり感染による苦痛と大勢の死を体験した時かもしれない。そしてその時にようやく、高病原性鳥インフルエンザで死に、殺された数億の鳥の苦しみに目を向け、彼らへの仕打ちを謝罪するのかもしれない。
だがそうなる前に行動することもできるはずだ。肉や卵を食べるのを止めることはそのまま工場型畜産の縮小に直結する。動物性食品の代替の選択肢は年々拡大している。今すぐにでも切り替えることが可能だ。一人一人が行動すれば次のパンデミックを防ぎ、それと同時にまだ続いている鳥社会のパンデミックでくるしむ家禽たちを救うことができる。
参照
We have to wake up: factory farms are breeding grounds for pandemics
「インフルエンザ」、「鳥インフルエンザ」と「新型インフルエンザ」の違い 更新日 H24.3.9
新型インフルエンザ事前準備・緊急対応体制の再構築 プレパンデミックワクチンの意義と必要性 国立感染症研究所インフルエンザウイルス研究センター長 田代 眞人
NHKスペシャル MEGA CRISIS 巨大危機3 ウイルス大感染時代
堀本泰介「感染爆発:インフルエンザパンデミック」ー公開講座「爆発」2017 東大TV
1 コメント
- Pingback: 48日齢 死体を見つけられない | ブロイラーに生まれたメイの50日

















